こんにちは。子ども科学ラボのさくらとあかりです。
今回は前回に引き続き化学の日特集ということで、モルを使った計算問題に挑戦していきます!!
目次
- 塩化ナトリウム NaCl …いわゆる お塩、食塩と呼ばれる物質。
- 硫酸 H₂SO₄ …強酸 大変危険。性質に関してはこちらをcheck! 【実験】 濃硫酸による砂糖の脱水 – YouTube
- メタンCH₄:温室効果ガスのひとつで、牛のゲップに含まれる。
- 窒素N₂:地球の大気中の約8割を占める気体。
- 酸素O₂:地球の大気中の約2割を占める気体。酸素さんいつもありがとう。
知らない名前の物質でも、大抵の場合原子量は教えてくれる問題が多いので安心です。
この3個を覚えておけば、余程性格の悪い問題でない限り大抵何とかなります。
質量(g)=モル質量(g/mol)×物質量(mol)
※モル質量・・・原子量にg/molつけた値。1molあたりの質量。
体積(L)=モル体積(22.4 L/mol)×物質量(mol)
※モル体積・・・標準状態での1molあたりの体積。
「標準状態」って書かれていたら22.4 L/mol。ちなみに体積は「L」で表すよ!
個数 =アボガドロ定数×物質量(mol)
※「アボガドロ定数」については1つ前の記事をcheck!
問題 0.300 molの塩化ナトリウム(NaCl)は何gか。 NaClのモル質量を 58.5 g/mol とする。
まず、この問題で何を聞かれているのかを整理しましょう。
簡単に一枚の画像で表すとこんな感じですね!
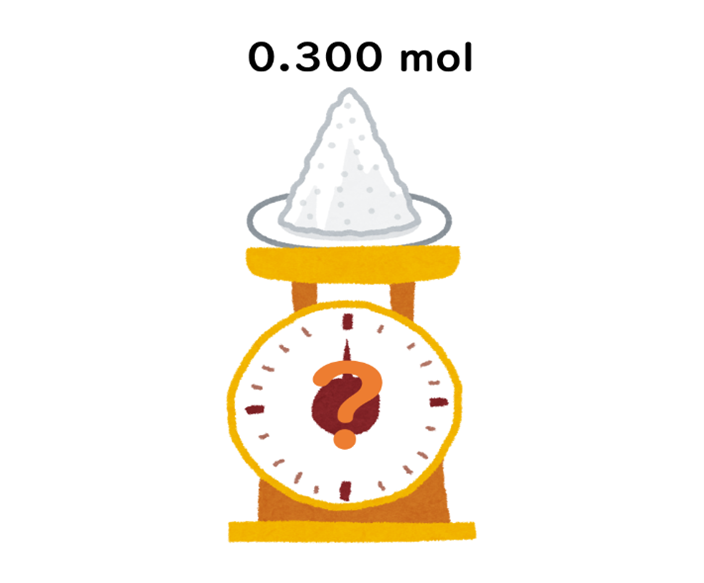
この問題では「食塩は何g?」ということを聞いています。
質量を求めるので、先程出てきた<質量を求めたいとき>を使います。
NaClのモル質量は58.5 g/molなので、これに物質量0.30 molを掛ければいいだけ!
思ったより簡単でしょ。
解答
NaClのモル質量は58.5gであるので、質量を求めると
0.300 (mol)×58.5 (g/mol)=17.55 (g)
有効数字3桁なので四捨五入して、17.6 g
公式を使って求めるのが正攻法ですが、実はmol計算には単位を使ってしまうという裏技があります。この方法だと、単位さえ覚えておけば別に公式をわざわざ覚える必要はありません。
質量を求める時は、モル質量の単位 g/molを分数の形にしてみるだけです。
質量の単位は gなので、分母のmolを消すにはmol(物質量)を掛け算する……みたいな感じ。
これは化学だけじゃなく、単位が絡む計算すべてに使えるのでおすすめです。
化学重要問題集 化学基礎・化学 数研出版
モルを使った計算問題はいかがだったでしょうか?? 次回はモルを使った計算の応用編です!お楽しみに。
余談ですが、近々小学生対象の実験教室をする予定です。興味ある方はぜひ各種SNSでご連絡ください。
Twitterとインスタもよろしくお願いします!


